Vliv teploty na rozpustnost látek
autor red. | kategorie Chemie 2. stupeň ZŠ
1 Vliv teploty na rozpustnost látek
Čas: 1 hodina
1.2 Pomůcky a chemikálie
5 zkumavek, trojnožka, síťka, kahan, kádinka, teploměr, váhy, lžička, filtrační aparatura, zápalky, dusičnan draselný KNO3, oxid vápenatý CaO, šťavelan amonný (NH4)2(COO)2, voda.
1.3 Princip
Připravíme přesycený roztok KNO3 a Ca(OH)2 za normální teploty. Se stoupající teplotou se v daném objemu vody rozpouští další množství KNO3 a při ochlazení se nadbytečné množství opět vyloučí. Vyloučené množství KNO3 je po zchladnutí v jednotlivých zkumavkách stále větší. Naopak rozpustnost Ca (OH)2 je při vyšší teplotě menší, proto důkaz na přítomnost kationtů Ca2+ je méně výrazný.
1.4 Postup
Úkol 1: Ověřte vliv teploty na rozpustnost KNO3
- Připravte si 5 zkumavek a aparaturu na zahřívání
- Do kádinky odměřte asi 50 ml vody.
- Navažte asi 75 g KNO3 a rozpusťte ho ve vodě.
- Určité množství soli zůstane nerozpuštěno.
- Směs zahřívejte a při teplotě 40 °C odeberte 5 ml roztoku do první zkumavky.
- Zahřívejte dále a při teplotě 60 °C, 80 °C, 100 °C postupně odebírejte vždy 5 ml roztoku do jednotlivých zkumavek.
- Nechte vychladnout.
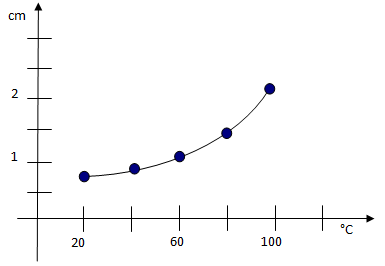
- Po zchladnutí zaznamenejte množství nerozpuštěné látky (změřte pravítkem výšku nerozpuštěné vrstvy) a vyneste do grafu.
Úkol 2: Ověřte rozpustnost Ca (OH)2 ve vodě.
- Rozpusťte lžičku CaO ve vodě.
- Vzniklou suspenzi Ca (OH)2 rozdělte na dvě části.
- Jednu část zfiltrujte do kádinky.
- Druhou část krátce zahřejte a rychle zfiltrujte.
- K oběma roztokům přidejte 2 – 3 kapky šťavelanu amonného.
- Porovnejte množství vzniklé sraženiny.
1.5 Otázky a úkoly pro žáky
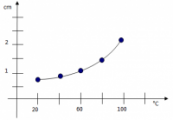
1) Na základě naměřených hodnot vypracujte grafickou závislost rozpustnosti na teplotě.
graf:
2) Zapište rovnicí děj při rozpouštění CaO ve vodě.
CaO + H2O Ca (OH)2
3) Jak byste dokázali, že roztok Ca(OH)2 má zásaditou reakci? (FFT zčervená)
4) Proč je množství vzniklé sraženiny šťavelanu vápenatého rozdílné? Jak byste zdůvodnili, že v jednom případě je množství sraženiny menší?
5) Najděte v literatuře informaci o kyselině šťavelové.
6) Napište aspoň tři způsoby, jakými můžete urychlit proces rozpouštění ve vodě.
(např. zvýšením teploty, mícháním, menší objem rozpouštěné látky, menší kousky rozpouštěné látky)
1.6 Metodické poznámky
Úkol 1:
Množství 75 g KNO3 je orientační (může být i více), viz tabulka rozpustnosti (ve 100 g vody):
|
teplota |
0 °C |
20 °C |
60 °C |
100 °C |
|
KNO3 |
13 g |
32 g |
110 g |
246 g |
- Důležité je rozpustit takové množství KNO3, aby vzniklý roztok byl při normální teplotě přesycený a aby byl přesycený alespoň při prvních teplotách odebírání.
- Se stoupající teplotou se v daném objemu vody rozpouští další množství KNO3 a při ochlazení se nadbytečné množství opět vyloučí.
- Vyloučené množství KNO3 je stále větší.
- Vyloučený KNO3 tvoří krásně viditelné krystaly.
Úkol 2:
Reakcí CaO s vodou vzniká málo rozpustný Ca(OH)2. Po přidání šťavelanu vzniká bílá sraženina šťavelanu vápenatého, který je ve vodě nerozpustný. Množství vzniklé sraženiny je závislé na přítomnosti kationtů Ca2+. Po přidání šťavelanu do roztoku, který byl zahříván, se vytvořilo méně sraženiny, protože Ca(OH)2 je ve vodě při vyšší teplotě hůře rozpustný.



Poslední komentáře