Hustota látek

autor PhDr. Jitka Soukupová | kategorie Fyzika Střední škola
1. Úkol: Experimenty na téma hustota kapalin
Seznámení se s pojmem hustota
Využití Archimédova zákona pro porovnání hustot
Experimentální porovnání hustot kapalin
Oxid uhličitý a změna hustoty nestejnorodé látky
Hustoměr, jeho využití a tvorba funkčního modelu hustoměru
Čas: 2 vyučovací hodiny
Pomůcky a materiál:
Pro jednu skupinu na jeden experiment:
- brčko, modelína, kancelářské sponky, nůžky, odměrný válec nebo jiná úzká průhledná nádoba, lihový fix, různé kapaliny
- čtyři průhledné láhve (stejné velikosti a stejného tvaru) s víčky, studená a teplá voda, potravinářské barvivo (vhodné jsou kombinace modrá + červená, žlutá + zelená, žlutá + červená atp.), hřebík, hrací nebo platební karta
- Průhledná vysoká nádoba, lžíce, různé kapaliny a pevné látky – med, sirup, kondenzované mléko, voda, tekuté mýdlo, olej, technický líh, dřevo, sklo, plast, korek, atp.
- průhledná sklenice, olej, ocet, jedlá soda, potravinářské barvivo, malá kádinka, kapátko
Hlavní a dílčí cíle:
seznámení se s pojmem hustota na základě experimentu
porovnávání hustoty kapaliny s využitím Archimédova zákona
aplikovat teoretické poznatky do praxe
systematizace teoretických poznatků na základě experimentu
schopnost realizovat a prezentovat experiment před publikem
řešení problémových úkolů a situací na základě experimentu
uvědomit si možnosti změny hustoty nestejnorodé látky
Mezipředmětové vztahy a přesahy:
matematika – výpočet objemu, hmotnosti a hustoty, aplikace Archimédova zákona
chemie – hustota kapalin, stejnorodá a nestejnorodá látka
biologie a ekologie – vliv hustoty na chování kapalin v přírodě, ekologické havárie, oxid uhličitý, chemické reakce
Klíčové kompetence:
Kompetence k učení – žák je efektivně využívá v procesu učení, plánuje a organizuje vlastní učení, vyhledává a třídí informace a na základě jejich pochopení, samostatně pozoruje a experimentuje, získané výsledky porovnává a vyvozuje z nich závěry pro další využití
Kompetence k řešení problémů - žák rozpozná a pochopí problém, přemýšlí o nesrovnalostech a jejich příčinách, promýšlí a plánuje způsob řešení problémů, ke kterým využívá vlastních úsudků a zkušeností, je schopen vyhledat informace vhodné k řešení problémů, využívá získané vědomosti a dovednosti, samostatně řeší problémy a vhodně volí způsoby řešení
Kompetence komunikativní - žák formuluje a vyjadřuje své myšlenky a názory účinně se zapojuje do diskuze obhajuje svůj názor, toleruje názor druhých lidí, avšak umí i vhodně argumentovat využívá informační a komunikační prostředky
Kompetence sociální a personální – žák spolupracuje ve skupině, zapojuje se do diskuze v malé skupině i v celé třídě, obhajuje svoje myšlenky a názory
Kompetence pracovní – žák používá bezpečně a účinně pomůcky, materiály a nástroje, dodržuje jasně vymezená pravidla dokáže se adaptovat na změněné nebo nové pracovní podmínky, využívá nabyté znalosti a zkušenosti získané v jednotlivých vzdělávacích oblastech v zájmu vlastního rozvoje
2 Obecný úvod k tématu:
Hustota látky je fyzikální veličina, která určuje, jaká je hmotnost jednotkového objemu látky.
Značka: r (ró) , jednotka: 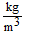 (kilogram na metr krychlový)
(kilogram na metr krychlový)
Hustotu kapalin můžeme určovat s využitím Archimédova zákona pomocí hustoměru, hustotu některých pevných látek, kapalin i plynů nalezneme v tabulkách a hustotu homogenního tělesa lze také určit výpočtem vycházejícím z definice hustoty. Jestliže se jedná o hmotnost látky v jednotkovém objemu, znamená to, že budeme při výpočtech vycházet ze vztahu 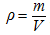 .
.
Archimédův zákon - těleso ponoření do kapaliny je nadlehčováno hydrostatickou vztlakovou silou, která je rovna tíze kapaliny tělesem vytlačené.
F vz = r g V, kde r je hustota kapaliny, V objem vytlačené kapaliny nebo ponořené části tělesa, g tíhové zrychlení.
Víte, že… Saturn jako jediná planeta sluneční soustavy má průměrnou hustotu menší než je hustota vody.
Voda v Mrtvém moři obsahuje z více než 27% sůl, zatímco v ostatních mořích a oceánech je sůl zastoupena 2–3%, takže má větší hustotu.
Motivační příběh: V blízkosti naší školy jsou dvě cukrárny. Majitelé, kteří oba prodávají za stejné ceny, zjistili, že do cukrárny pana Poctivého chodí samí výborní fyzici a cukrárně pana Nepoctivého se vyhýbají, zatímco ti, které fyzika nezajímá a nebaví, chodí k panu Nepoctivému. A my jsme zjistili proč – minerálka u pana Poctivého i Nepoctivého sice stojí stejně, je jí i stejné množství, ale nechutná stejně. Jak ale panu Nepoctivému dokázat, že místo minerálky nalévá vodu? Stačí do obou skleniček nasypat špetku soli nebo pár hrozinek. Zkuste to a vysvětlete.
Pracovní postup (v bodech):
- Připravíme pomůcky dle seznamu
- V bodech sepíšeme pracovní postup
- Realizujeme experiment
- Vysvětlíme výsledky experimentu
- Diskutujeme a řešíme zadané úkoly
1. Poměrový hustoměr
Pomůcky: brčko, modelína, kancelářské sponky, nůžky, odměrný válec nebo jiná úzká průhledná nádoba, lihový fix, různé kapaliny
Postup: Do spodní části brčka vtlačíme modelínu tak, aby bylo utěsněné. Do modelíny upevníme zespodu kancelářskou sponku, která funguje jako „kýl“, tj. jejím nakloněním v modelíně upravíme polohu těžiště brčka a stabilizujeme je ve svislé poloze. Takto upravené brčko ponoříme do odměrného válce, ve kterém je voda. Ubíráme nebo přidáváme modelínu tak, aby bylo brčko ponořené zhruba z poloviny. Teď už stačí jen měnit kapaliny a fixem vyznačit příslušné hodnoty. Pro poměřování jsou vhodné například olej, technický líh, šťáva, slaná voda, případně různě tučná mléka, smetana a acidofilní mléko.

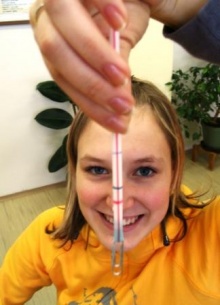
Praxe: V praxi se pro měření hustoty kapalin používají kalibrované hustoměry s různým rozsahem stupnic. Význam mají v potravinářství, automobilovém průmyslu i dalších odvětvích – umožňují velmi přesně určit hustotu alkoholu, hustotu benzínu a podobně.
Vysvětlení: Při ustálení ponoru brčka do kapaliny nastává situace, kdy jsou v rovnováze tíhová a vztlaková síla působící na brčko. Hustoměr je nadlehčován vztlakovou silou, která je rovna tíze kapaliny mající objem ponořené části brčka. Tíha vytlačené kapaliny závisí na objemu ponořené části hustoměru a na hustotě kapaliny. Jestliže hustoměr ponoříme do kapaliny o vyšší hustotě, pro dosažení potřebné vztlakové síly stačí, aby hustoměr vytlačil menší objem kapaliny. Proto se hustoměr méně ponoří. V kapalině o nižší hustotě je tomu naopak. S rostoucí hustotou kapaliny se brčko ponoří méně, takže nejníže jsou na našem poměrovém hustoměru vyznačeny látky s nejvyšší hustotou.
Úkoly k pokusu:
- Uspořádejte aspoň čtyři vámi zvolené kapaliny podle hustoty, v tabulkách nebo na internetu vyhledejte přibližné hustoty použitých kapalin a porovnejte výsledky experimentu s tabulkovými hodnotami.
- Vyznačte hloubku ponoru hustoměru pro dvě různé kapaliny a z Archimédova zákona zjistěte, jak velkou vztlakovou silou je v daných situacích brčko nadlehčováno.
- Uveďte aspoň tři jevy, kde se s daným principem setkáte.
2. Barevná voda pokaždé jinak, aneb kde je teplá a kde studená voda
Pomůcky: čtyři průhledné láhve (stejné velikosti a stejného tvaru) s víčky, studená a teplá voda, potravinářské barvivo (vhodné jsou kombinace modrá + červená, žlutá + zelená, žlutá + červená atp.), hřebík, hrací nebo platební karta
Postup: Udělejte (například horkým hřebíkem) do víček ve stejném místě otvory o průměru 0,5–1 cm. Do dvou lahví nalijte teplou a do dvou studenou vodu. Teplou vodu obarvěte v obou láhvích jednou barvou, studenou vodu druhou. Láhve uzavřete upravenými víčky a pomocí karty obraťte vždy dvě a dvě na sebe tak, aby jednou byla teplá voda ve spodní láhvi a studená nahoře a podruhé naopak. Kartu opatrně vyjměte.


Praxe: Tento jev je možné pozorovat v přírodě – voda s nejvyšší hustotou se drží u dna – jedná se o vodu o teplotě cca 4 stupně Celsia. Umožňuje život vodní fauny a flóry v zimě v zamrzlých řekách a rybnících. Stejně tak mořské proudy teplé se nacházejí při hladině moří a oceánů, studené naopak u dna.
Vysvětlení: V případě, že je ve spodní láhvi studená a v horní láhvi teplá voda, se obarvené kapaliny nesmísí a barvy zůstanou oddělené. V případě, že ve spodní láhvi je voda teplá a nahoře studená, dojde k promísení barev a vzniku fialové, modré či oranžové tekutiny podle kombinací použitých barev. Teplá voda má menší hustotu než voda studená, proto se v prvním případě drží nahoře na svém původním místě a ve druhém případě se dostává nahoru a studená voda klesá ke dnu a barviva se prouděním smísí.
Úkoly k pokusu:
1. Vyzkoušejte si podobný experiment s jednou láhví plnou vody a druhou plnou oleje.
Co se v jednotlivých situacích s vodou a olejem stane a proč?
2. Navrhněte praktické využité daného jevu, případně uveďte zařízení, která tento princip využívají.
3. V literatuře a na internetu zjistěte základní informace související s anomálií vody a prezentujte je.
3. Barevný koktejl
Pomůcky: Průhledná vysoká nádoba, lžíce, různé kapaliny a pevné látky – med, sirup, kondenzované mléko, voda, tekuté mýdlo, olej, technický líh, dřevo, sklo, plast, korek, atp.
Postup: Do nádoby po stěně pomocí lžičky postupně naléváme jednotlivé vrstvy kapalin podle hustoty.
Takto nalité kapaliny se téměř nesmísí a vytvoří barevné vrstvy. Pro lepší barevný efekt můžeme líh a vodu obarvit potravinářským barvivem.
Následně vkládáme do kapaliny kousky korku, dřeva, plastu atp. Ty se v závislosti na hustotě zastaví mezi různými vrstvami kapalin.


Praxe: V praxi často pozorujeme olejové či ropné skvrny na vodě. Jedná se o dvě kapaliny, které se navzájem nemísí a zároveň se liší svojí hustotou.
Vysvětlení: Některé kapaliny se navzájem nemísí a ty ostatní se při opatrném nalévání smísí pouze nepatrně na svých rozhraních. Tím kapaliny vytvoří postupně barevné vrstvy. V jednotlivých vrstvách jsou kapaliny uspořádány podle hustoty od kapaliny s nejvyšší hustotou u dna sklenice po kapalinu s nejmenší hustotou u okraje sklenice.
Úkoly k pokusu:
1. Porovnejte hustoty použitých kapalin výpočtem – z určené hmotnosti a objemu a experimentálně – z pořadí jednotlivých vrstev barevného koktejlu.
2. Ve které části roztoku se zastaví dřevěná zápalka? Proč, co z toho vyplývá pro hustotu dřeva?
3. Určete hustotu dřeva v intervalu podle ponoření do příslušných kapalin, výpočtem z určené hmotnosti a objemu a nalezněte v tabulkách.
4. Lávová lampa
Pomůcky: sklenice, olej, ocet, soda, potravinářské barvy, kádinka, kapátko
Postup: Do sklenice nalijeme olej. Následně do něj nasypeme polévkovou lžíci jedlé sody. V kádince rozmícháme potravinářskou barvu s octem. Kapátkem přidáme obarvený ocet do sklenice s olejem a sodou.


Vysvětlení: Ocet reaguje u dna se sodou za vzniku oxidu uhličitého, což se začne projevovat uvolňováním plynu oxidu uhličitého. Bublinky oxidu uhličitého mají výrazně nižší hustotu než olej. Proto s sebou vynášejí obarvené kapičky octa k povrchu. Zde bubliny oxidu uhličitého praskají, protože oxid uhličitý se uvolňuje do okolí a obarvený ocet klesá zpět ke dnu, protože jeho hustota je větší než hustota oleje. U dna opět reaguje se sodou a celý cyklus se opakuje.
Praxe: V praxi se užívá změny hustoty nestejnorodých látek při ponoru lodí ve sladkovodní či mořské vodě, při vytlačování či nasávání vody ponorkou, do hloubky se podobným způsobem ponořují medúzy.
Modifikace: Při velkém množství sody a koncentrovaného octa můžeme ve sklenici pozorovat „tornádo“ – proud bublinek oxidu uhličitého je díky rychlé reakci tak intenzivní, že se nám jeví jako velký barevný vír tornáda. Obdobným způsobem můžeme pozorovat hrozinky, tabulku čokolády, kivi či dokonce broskev, která ve sklenici minerálky či jiné sycené limonády putuje nahoru a dolů díky tomu, že je obalena bublinkami oxidu uhličitého.

 Pracovní listy
Pracovní listy

Poslední komentáře